Nel febbraio 2026, la FDA implementerà il Quality Management System Regulation (QMSR), un cambiamento epocale che ridefinisce il modo in cui vengono condotti gli audit dei dispositivi medici negli Stati Uniti. Per gli auditor ISO 13485, questo rappresenta sia una grande opportunità professionale sia una sfida, richiedendo una comprensione approfondita dell’integrazione tra standard internazionale e regolazione statunitense.
Cos’è il QMSR e perché cambia l’audit nei dispositivi medici
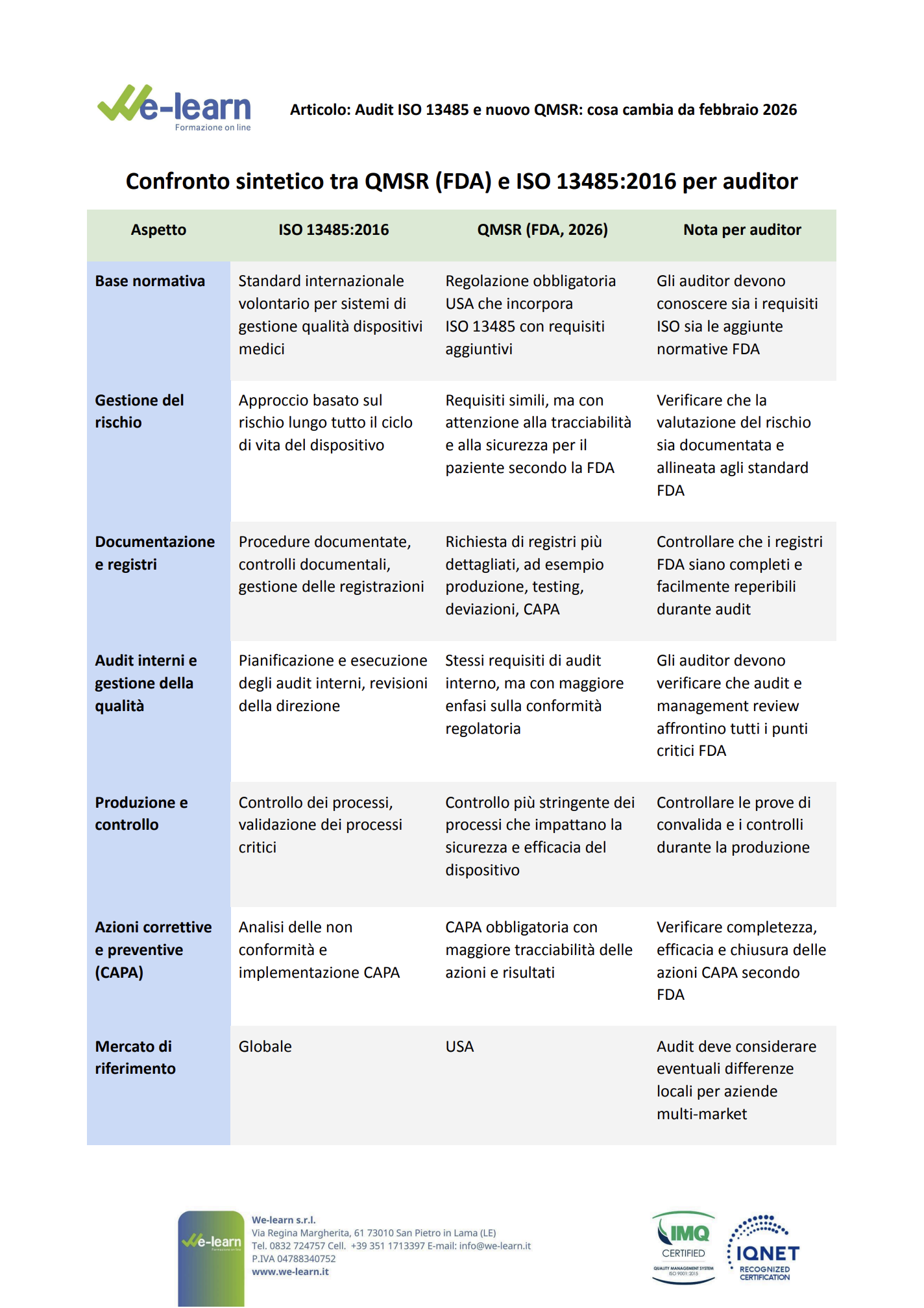
Il QMSR sostituisce la vecchia Quality System Regulation (21 CFR Part 820) e incorpora direttamente i requisiti della ISO 13485:2016. In pratica, la FDA allinea le ispezioni statunitensi ai principi ISO 13485, con alcune integrazioni specifiche per la conformità regolatoria locale.
Questo significa che le aziende che operano negli USA dovranno gestire i propri sistemi di qualità secondo una logica ISO 13485-based, ma con alcuni requisiti aggiuntivi che riflettono la normativa FDA. Gli auditor devono quindi saper interpretare e verificare entrambi i livelli di conformità.
Impatto pratico sugli auditor ISO 13485
Il cambiamento comporta implicazioni dirette per chi conduce audit:
- Comprensione approfondita della normativa FDA 2021: oltre ai requisiti ISO, gli auditor devono riconoscere le differenze regolatorie inserite nel QMSR.
- Audit integrati: i controlli sul sistema di gestione della qualità devono verificare sia la conformità ISO 13485 sia l’aderenza ai requisiti FDA specifici, come gestione dei documenti, registri di produzione e revisioni di management review.
- Approccio globale: in contesti multinazionali, gli audit dovranno considerare la coerenza tra sistemi di qualità locali e i requisiti globali, garantendo una visione completa del rischio e della conformità.
Documento allegato
Come prepararsi alle nuove sfide
Ecco alcune strategie concrete per gli auditor che vogliono affrontare il QMSR con successo:
- Formazione integrata: approfondire i requisiti ISO 13485 nel contesto del QMSR, comprese le specificità FDA.
- Audit simulati: esercitazioni pratiche su casi reali per evidenziare differenze tra audit ISO 13485 standard e audit QMSR.
- Check-list evolute: predisporre strumenti di controllo che includano sia i requisiti ISO sia le aggiunte regolatorie, evitando lacune durante le ispezioni.
- Aggiornamento continuo: seguire le linee guida FDA e le best practice internazionali per mantenere alta la competenza e l’efficacia dell’audit.
Conclusione
L’entrata in vigore del QMSR della FDA segna un punto di svolta per il settore dei dispositivi medici e per la professione di auditor ISO 13485. Prepararsi oggi significa anticipare le esigenze del mercato, offrire valore concreto alle aziende e consolidare la propria posizione come professionista altamente qualificato nel campo della qualità e della compliance regolatoria.
Gli auditor che sapranno integrare le competenze ISO 13485 con la conoscenza del nuovo QMSR saranno i protagonisti dei prossimi anni, diventando veri partner strategici per le aziende globali del settore medicale.